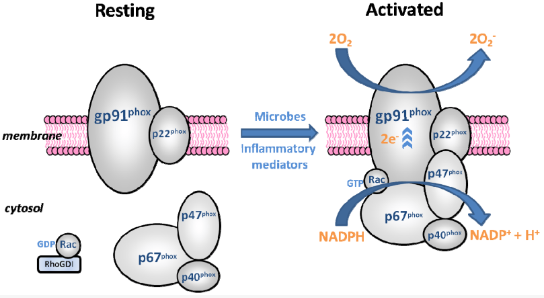
인체 내에서 활성산소가 만들어지는 가장 대표적인 기전이 면역반응을 위한 NADPH oxidase 촉매활동과 ATP 생산을 하기 위한 세포 내 산화적 인산화, 요산 배출경로 등임을 이전 글에서 살펴보았다. 이 들 모두 우리의 건강한 생명보존을 위해 반드시 필요한 반응들이다. 외부로부터 침입한 박테리아등을 비롯한 세균들을 살상하기 위한 강력한 살상무기가 필요해진 우리 인체는 NADPH oxidase 복합체를 활용하여 다양한 활성산소들을 생산해 낸다. 이를 호흡폭발(respiratory burst)또는 산화폭발(oxidative burst)라고 한다. 식세포가 집어삼킨 세균을 녹여버리기 위한 라디칼 생산 공정을 자세히 살펴보자.
백혈구의 식균작용 (phagocytosis), 1차 방어선.
먼저, 호흡폭발이 일어나는 백혈구의 대식세포(Macrophage)와 호중구(Neutrophil)의 식균작용(phagocytosis) 과정을 아주 간단히 살펴보자. 백혈구의 많게는 70%이상을 차지하는 호중구와 대식세포는 내 몸의 일부가 아닌 외부로부터 박테리아나 바이러스들이 침입했을때 가장 먼저 지체없이 반응하는 선천면역 중 제1차 방어선이다. 이들은 침입한 병원체 근처로 재빠르게 이동하여 통째로 이들을 포식 즉 집어 삼킨 후 액체로 가득 찬 동그란 낭(vesicle)인 파고솜(phagosome)으로 주변을 둘러싸 포식낭을 만든다. 이후, 이 병균체를 가수분해하여 소화할 수 있는 효소와 녹여서 살상할 수 있는 활성산소종 ROS를 만들 수 있는 리소좀(lysosomes)과 융합하여 파고리소좀(phagolysosomes)을 형성한다. 이 안에서 병원체를 소화 및 처리한 후 이미노산과 같은 유용한 분자는 세포질로 보내 재활용하고 나머지 수용성 찌꺼기는 세포밖으로 버린다. 임무가 끝난 파고리소좀은 해체된다.
이 과정중 파고리소좀 안에서 NADPH 산화효소가 ROS들을 생산하여 병원체와 바이러스 등을 살상하는 파괴적인 항균활동을 하는 것이다.
NADPH 산화효소
NADPH와 NADPH oxidase
NADPH(Nicotinamide adenine dinucleotide phosphate)는세포내 산화환원 반응에 관여하는 조효소로서 고에너지 전자를 운반하고 전달하는 전자 전달 매체로 이해할 수 있다. 수많은 생화학 반응에서 중요한 보조 인자로서 역할하며 주로 다른 분자에게 전자를 기증하는 환원제 기능을 한다. 참고로, 에너지를 생성하는 이화 과정, 즉 해당과정, TCA cycle, 세포 호흡(산화적 인산화 또는 전자 수송 사슬)과 같은 과정에서 전자운반체 역할을 하는 NADH 조효소와 매우 비슷하다. 이 둘 모두 비타민 B3 니아신으로부터 만들어져 세포 대사와 산화환원 균형에 필수적인 역할을 한다.
NADPH 산화 촉매 효소는 NADPH를 전자 공여체로 이용하여 산소에게 전자를 주고(환원시켜) 슈퍼옥사이드라디칼이나 과산화수소등의 ROS 활성산소종이 생성되도록 촉매하는 효소 복합체이다.
NOX 패밀리
NADPH oxidase(줄여 NOX, Nox라고 부름) 동족체(homologues)패밀리에는 Nox1 ~ 5및 이중 산화 효소인 Duox1 및 Duox2 (Nox6 및 Nox7)를 포함하여 현재 7개가 발견되었으며[1], 이들은 각각 다양한 기능과 활성화 메커니즘을 갖고 세포와 조직에 광범위하게 분포되어 있다. 숙주 방어(Nox2), 귀안에 이석 형성(Nox3), 갑상선 호르몬의 요오드화(Duox2), 혈관 긴장 조절(Nox2) 등이 이들의 역할의 예이다[2]. Nox 단백질은 세포 성장, 분화, 세포사멸 및 세포골격 리모델링을 포함한 많은 기본적인 생리학적 과정 조절에도 관여하는 것으로 나타났다.
그렇다면 NOX에 의해 생성된 ROS는 어떤 역할을 하는가. 크게 2가지로 볼 수 있는데, 첫 번째는 오랫동안 잘 알려진 대로 숙주 방어를 위한 전통적인 식세포로서의 역할이고 2번째는 최근에 와서야 밝혀져 관심을 모으고 있는 신호전달과 관련된 역할이다. NOX를 통해 발생된 ROS가 단백질과 특이적이고 가역적으로 반응하여 단백질의 활성, 국소화 및 반감기를 변경할 수 있으며 비식세포에서 ROS가 종종 키나제 및 포스파타제 활성의 조절 또는 유전자 전사를 통해 신호 전달 조절에 중요한 역할을 한다는 것도 밝혀지고 있다. ROS 중에서도 음전하를 가져 생물학적 막을 넘나들며 이동하기 힘든 슈퍼옥사이드라디칼과는 달리 H2O2는 막횡단이 가능하며 상대적으로 안정적이다. H2O2에 의한 티올(thiol) 산화는 다양한 생리학적 결과를 초래함으로써 수많은 신호전달 경로에 관여하는 것으로 나타났다. 신호전달 분자로서의 H2O2의 역할은 다른 글에서 좀 더 자세히 다룬다. 하지만, NOX의 가장 큰 역할은, 또는 주요한 기능은 역시 '활성산소 생성'이다.
활성산소를 제조하기 위한 메커니즘.
플라보사이토크롬(flavocytochrome) b558 복합체와 4개의 하위 단위
식세포 NADPH 산화효소 복합체를 이루는 구성원들을 보자. 이 촉매 복합체의 중심에는 당단백질 gp91phox이 있다. phox는 phagocytic oxidase을 줄인 것으로 식세포 촉매효소를 의미한다. gp91phox는 세포막에 결합되어 있으며 NOX2라는 별명으로 더 잘 알려져 있다. 이는 그보다 좀 작은 p22 phox 단백질과 결합하여 사실상 이 촉매작용의 가장 핵심이고 그 중심에 있다고 할 수 있는 플라보사이토크롬(flavocytochrome) b558복합체(즉, gp91phox + p22 phox)를 형성한다.
플라보사이토크롬(flavocytochrome) b558 복합체 외에 또 하나의 하위 단위 그룹은 이 복합체와 떨어져 막이 아닌 세포질에 존재한다. p47phox, p67phox, p40phox, 그리고 세포신호전달 G-단백질 Rac 및 Rap1A GTPases의 4개 하위 단위가 그들이다. 이들은 휴지기에 세포질에서 안정된 상태로 떨어져 존재하다가, 세균 또는 곰팡이 감염, 염증성 사이토카인 및 기타 신호 분자와 같은 자극에 응답하여 촉매가 활성화되어야만 곧바로 막으로 이동하여 플라보사이토크롬 b558에 도킹한다. 이 두 그룹 간의 물리적 공간적 분리는 자칫 활성산소가 무분별하게 과다 생산되는 것을 미연에 방지하기 위한 우리 인체의 세심한 노력이라 할 수 있다. 실제로 p40 phox와 p47 phox는 원래 자가 억제(self-inhibited) 상태이기 때문에 활성화되려면 인산화의 과정을 거쳐야 만한다. 적절한 신호가 수신되었을 때에만 산화효소 하위 단위가 조립되어 활성 효소 복합체를 형성하도록 보장하는 복잡한 시스템은 오랜 시간을 통해 진화하였을 것으로 보인다.
슈퍼옥사이드라디칼의 생성
파고리소좀 막에서 플라보사이토크롬(flavocytochrome) b558 복합체를 중심으로 하여 6개의 단위가 모두 합체되어 조립이 완성되면, 활성산소 제조에 착수할 준비가 끝난 것이다. 이제 세포질의 NADPH로부터 전자를 받아 플라보사이토크롬 b558 내부에서 세포막의 안과 밖을 번갈아 횡단하는 6개의 나선 구조를 거치며 전자를 이동시키는 것이다. 이 반응을 촉매 하는 NADPH는 전자 2개와 양성자 1개를 방출하고 산화화여 NADP + 로 전환된다. 양성자는 세포질에 남아 있는 반면, 두 개의 전자는 식세포막을 통해 운반되어 최종적으로 두 개의 산소 분자에 결합하고 세포 외 또는 식세포 내 공간에서 두 개의 슈퍼옥사이드라디칼을 만들어 낸다. 이들은 식세포에 의해 포획된 병원체의 파괴에 투입되는 강력한 항균제가 된다.
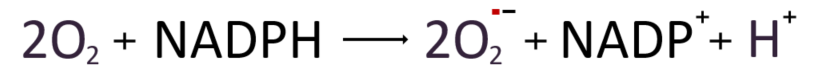
과산화수소(H2O2)의 생성
생성된 슈퍼옥사이드라디칼은 자연적으로 주변으로부터 전자를 받거나, 혹은 SOD(Superoxide dismutase)의 개입으로 과산화수소와 물로 전환된다.
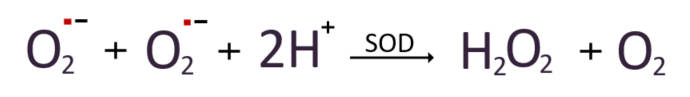
과산화수소를 안전한 물로 전환시키는 항산화 촉매제는 다양하게 존재한다. 대표적으로 글루타티온 퍼록시다제와 카탈라제가 있다.
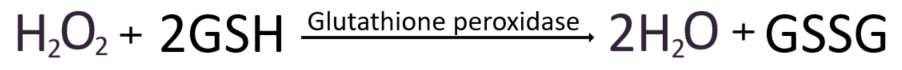

더욱 강력한 ROS: 차아염소산과 수산화라디칼
과산화수소가 항산화제들을 만나 안전한 물로 전환될 수도 있지만, 만일 염소음이온(Cl-)과 결합된다면 강력한 살충효과를 보일 수 있는 차아염소산(Hypochlorous acid)이 생성된다. 이 과정은 마이엘로퍼록시다제라는 효소에 의해 촉매 된다. 차아염소산은 강력한 살충제로서 우리 일반가정에서 세탁용 표백제로 쓰는 성분이기도 하다. 그러나 차아염소산이 침입한 병원군 퇴치를 더욱 촉진시켜주는 든든한 아군이기도 한 반면, 종종 세포밖으로 유출된 MPO가 부적절하게 차아염소산을생산하여 숙주 조직에 손상을 입히고 질병 발병을 촉진하는 등 특히 만성 염증반응에 부정적인 역할을 하여 문제를 일으키기도 한다.
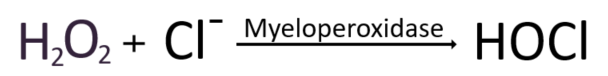
슈퍼옥사이드라디칼, 과산화수소, 그리고 차아염소산까지 다양한 ROS가 생성되어 식세포의 세균제거를 확실히 수행해 낸다. 그런데 여기서 그치지 않고, 우리가 알고 있는 가장 치명적이고 강력한 ROS라 할 수 있는 수산화라디칼 역시 이 과정에서 생성될 수 있다. 주변의 철이나 구리양이온이 있을 경우, 과산화수소는 이들과 반응하여 수산화라디칼을 형성한다. 이를 펜톤 반응과 하버-바이스반응이라고 한다.

우리 인체를 외부의 해로운 병원균으로부터 방어하기 위한 면역작용의 하나로 ROS를 생산해 내는 메커니즘이지만, 만일다양한 종류의 ROS가 필요이상으로 지나치게 많이 생산된다면 활성산소와 항산화효소 간의 균형이 깨어져 산화스트레스 상태에 빠질 수 있다. 따라서 이러한 선의의 목적을 가진 의도적 ROS생산이라 할지라도 이들을 제어하고 콘드롤 하기 위한 항산화효소의 역할이 매우 중요함을 알 수 있다.
NOX유전자변이 만성육아종(Chronic Granulomatous Disease, CGD)
ROS를 통한 항균면역반응을 살펴보았는데, 이 반응의 출발점은 NADPH 산화효소이다. 면역 측면에서 이 효소의 정상적인 발현이 얼마나 중요한지는 만성육아종(Chronic Granulomatous Disease, CGD)이라는 무서운 유전자질병을 통해 추측할 수 있다. 이는 NOX를 구성하는 gp91phox 등의 단백질 코딩에 유전적 변이가 발생하여 NOX가 ROS를 정상적으로 생산하지 못하는 유전적 면역계 질환으로서, 병원체를 살상하지 못하게 되어 병원체를 몇 겹으로 둘러쌈으로써 살상해 보고자 하는 과정에서 백혈구 덩어리를 형성하기도 하지만 ROS만큼 효과를 보지 못하고 생명을 위협하는 감염이 끊임없이 재발하여 결국 목숨을 잃을 수 도 있는 무서운 질환이다. 면역방어체계에서 ROS가 없어서는 안 될 중추적 역할을 하고 있음을 보여주는 한 예이다.
[참고자료]
[1] NADPH oxidases: an overview from structure to innate immunity-associated pathologies
https://www.nature.com/articles/cmi201489
[2] Nox proteins in signal transduction
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2763943/
Defining the molecular role of gp91phox in the immune manifestation of acute allergic asthma using a preclinical murine model.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3266200/
Activation and assembly of the NADPH oxidase: a structural perspective
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1134858/
NADPH Oxidase as a Therapeutic Target for Neuroprotection against Ischaemic Stroke: Future Perspectives
https://www.mdpi.com/2076-3425/3/2/561
NADPH Oxidases (NOX): An Overview from Discovery, Molecular Mechanisms to Physiology and Pathology
https://www.mdpi.com/2076-3921/10/6/890
Chronic Granulomatous Disease
https://emedicine.medscape.com/article/1116022-overview?form=fpf
'활성산소(ROS)관련' 카테고리의 다른 글
| ROS: 자유라디칼은 필요악(necessary evil)인가. (0) | 2024.03.10 |
|---|---|
| ROS: 신호전달물질로서의 ROS (1) | 2024.03.10 |
| ROS: 활성산소는 어디서 만들어지는가 (0) | 2024.03.10 |
| ROS: 가장 강력한 라디칼: 수산화라디칼(ft 지질과산화) (1) | 2024.03.10 |
| ROS: 활성산소종(Reactive Oxygen Species) (0) | 2024.01.23 |